En este segundo capítulo del Servicio de Resonancia Magnética de Investigación queremos hablaros en una pequeña introducción de la imagen funcional por Resonancia Magnética, la cual permite estudiar la funcionalidad, conectividad y actividad cerebral.
A dia de hoy, hay una gran variedad de estudios de fMRI en los que se varía el tipo de anestesia, las secuencias de adquisición, los paradigmas empleados; todo para definir/o unificar un buen diseño experimental, ya que en imagen animal siguen surgiendo controversias tanto en el método de análisis como el tratamiento de las imágenes. Son muchos los artículos publicados y solo 868 los que se han considerado relevantes para escribir la revisión en la que se basa este documento. La revisión se ha hecho en función del tipo de estudio: Resting State, neuromodulación opto/quimiogenética provocada por fármacos, estimulación profunda, o estimulaciones provocadas (por bloques o por eventos con estimulación sensorial, o gaseosa, etc.). Se ha escrito también sobre la especie animal, número de animales, la preparación del animal: despierto, anestesiado con y sin ventilación, el nivel de anestesia durante la adquisición, el campo magnético, la secuencia de fMRI y el contraste, y los programas de pre-procesamiento.
A continuación se detalla alguno de los puntos más relevantes de la revisión.
El diseño experimental
- Imagen fMRI con estímulos provocados
Se pueden emplear estímulos externos (p.ejemplo: estimulación eléctrica de la pata delantera) o también internamente (estimulación profunda cerebral (DBS) y optogénetica). Los estímulos se pueden aplicar en bloques o en un diseño de eventos relacionados. En el primero se alternan condiciones de estimulación +/-, mientras que en el segundo se aplica un pequeño estímulo en varios intervalos.
En la estimulación por bloques se estudia la frecuencia relacionada con las respuestas producidas y en el de estímulos relacionados se estudia la duración del tiempo/respuesta y así poder valorar la conectividad funcional independiente de la frecuencia.
Las altas frecuencias aumentarán la entrada de estímulos por unidad de tiempo, aumentando la señal y la habilidad de detectar respuestas provocadas. Esta estimulación eléctrica u óptica, puede provocar daños en el tejido (calentamiento), artefactos y efectos no específicos. También puede cambiar la fisiología básica y por tanto alterar la respuesta fMRI.
- Conectividad funcional MRI (RS-FC: Resting State- functional Connectivity)
Mediante esta técnica, los datos que se recogen son sin estimulación. Se emplea para investigar la sincronización de las señales que varían espontáneamente en una combinación anatómica y funcional en unas áreas de cerebro determinados.
El empleo de esta técnica se ha incrementado a lo largo de esta última década. En los estudios recientes, sugieren que los componentes de la red cerebral muestran unas propiedades no estacionarias, el tiempo de repetición tiene que ser corto (1seg) para recoger las fluctuaciones y detectar estos cambios. El tiempo de adquisición total deberá ser lo suficientemente largo para adquirir un mínimo de 300 imágenes.
También hay que tener en cuenta, que si se aplica una modulación/estimulación hay que añadir un tiempo durante los periodos de transición y el resting state para permitir una conectividad estable, y por tanto, un tiempo de reposo que permita que cada manipulación pueda ser agrupada separadamente para tener en cuenta las potenciales neuroadaptaciones. Hay que trabajar con cuidado con la fisiología y la anestesia para estar seguros de que se consigue la máxima detección de la señal.
- Optogenética
Permite una estimulación en una población específica celular y/o anatómica pero requiere una metodología muy rigurosa y controles adicionales. Las opsinas son las proteínas que actúan como canales/bombas que son activadas por la luz. Hay varias opsinas que pueden ser elegidas para excitar las células ópticamente, entre ellas la más comúnmente utilizada es la ChR2 que se activa con luz roja y variantes ultra rápidas capaces de aumentar la frecuencia a 200Hz. También hay opsinas que producen una inhibición celular, pero su aplicación a la fMRI está limitada porque requieren largos periodos de iluminación que producen artefactos relacionados con el calor, y donde los animales anestesiados o sedados dan bajas señales de actividad. La inyección de virus o la expresión de genes pueden cambiar potencialmente la función cerebral y la luz puede inducir calor y con ellos artefactos en al señal de IRM, daño tisular y efectos no específicos que son críticos para caracterizar la expresión de opsinas.
- Quimiogenética
Inicialmente llamada farmacogénetica, se emplean ligandos farmacológicamente inertes para producir una estimulación en unos receptores específicos sobre una población neuronal específica. Los primeros intentos para combinar esta aproximación con la fMRI han involucrado la expresión regional de receptores de proteínas G acopladas farmacologícamente activadas. Esta metodología al igual que en la optogenética, requiere una metodología muy rigurosa para controlar los efectos no deseados.
- fMRI con fármacos
La modulación del cerebro por fármacos durante la fMRI es ampliamente utilizada para estudiar los efectos globales de los compuestos en el sistema neurotransmisor diana. No requiere cirugía y es apta para identificar los cambios globales o regionales de la función asociados a las nuevas terapias que actúan sobre las enfermedades cerebrales producidas a nivel de neurotransmisores o para mapear el efecto de los neuromodulares administrados. Sin embargo, esta metodología no es la más apropiada para estudios dinámicos y repetitivos ya que los efectos son dependientes de la difusión y de la cinética del receptor que pueden llevar a una desensibilización y baja regulación del receptor. Hay que tener en cuenta los efectos dosis-respuesta y la farmacocinética del compuesto en el diseño experimental. Muchos agentes tienen efectos sistémicos que pueden afectar a la fisiología del animal y a la señal BOLD. Algunos fármacos tienen efectos directos en el endotelio vascular del cerebro que podría alterar las propiedades de la respuesta hemodinámica.
Es muy importante llevar un control y una monitorización de la fisiología del animal y usar una dosis apropiada para controlar los efectos secundarios. El aumento del flujo y volumen sanguíneo y un incremento en la presión sanguínea producido en las infusiones puede alterar la señal de MRI.
Factores a tener en cuenta:
- Tipo de especie, el tamaño de muestra, sexo del animal:
En la revisión llevada a cabo los estudios que se han realizado han sido sobre muchas especies, siendo la rata la más utilizada, concretamente la especie Sprague Dawley
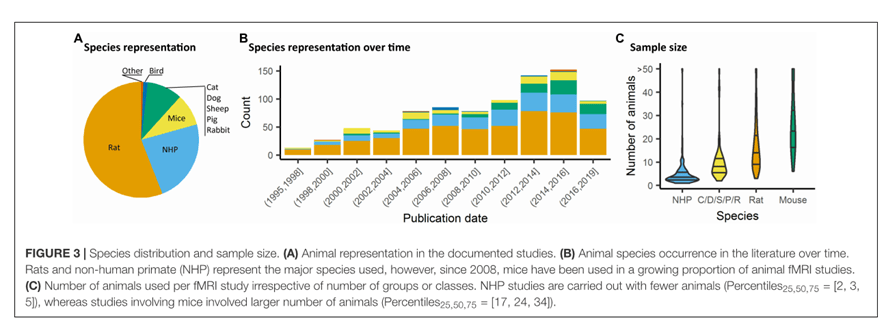
La descripción de cada arquitectura funcional en cada especie se ha basado en una variedad de análisis, adquisiciones y protocolos con/sin anestesia. Esta falta de estandarización interespecie es debida al tamaño del cerebro, a las diferentes respuestas frente a la anestesia, y a las organizaciones anatómicas observadas entre los mamíferos.
- Preparación del animal y anestesia
Influencia del movimiento y el estrés.
En fMRI la información obtenida es debida a los cambios temporales en los parámetros hemodinámicos (oxigenación de la sangre: contraste BOLD, volumen sanguíneo cerebral CBV, o flujo sanguíneo cerebral (CBF). Las señales fMRI explicarían la activación neuronal a través de la evaluación de la respuesta hemodinámica, por ejemplo la adaptibilidad de los capilares locales para entregar oxígeno a las neuronas activas a una velocidad mayor que las neuronas inactivas. La señal BOLD es el parámetro más estudiado en fMRI, es dependiente de los niveles relativos de oxihemoglobina y deoxihemoglobina, modulados a su vez por los volúmenes y el flujo de sangre a nivel local.
Además las adquisiciones de fMRI son muy sensibles al movimiento del sujeto, especialmente en los límites del tejido. En la mayoría de los estudios, los animales son anestesiados para evitar el movimiento, se sujetan también a través de barras en los oídos y en los dientes. Pero también hay estudios con el animal despierto, empleando dispositivos que les retenga en un espacio más limitado utilizando barras que sujeten la cabeza y que no les cause ningún tipo de daño ni malestar. Pero por mucho que se fije el animal siempre hay un movimiento que es el de la respiración; para ello, se puede recurrir a la ventilación mecánica del animal, de esta manera se reduce de manera considerable el artefacto de movimiento durante la adquisición de la señal. Otra fuente de ruido y mala interpretación de la señal, es el producido por el latido cardiaco que induce pequeñas fluctuaciones en la señal BOLD a bajas frecuencias.
En algunos casos, la respuesta cardiaca puede enmascarar la respuesta neuronal, especialmente la respuesta a un estimulo de estrés.
Impacto de la anestesia en la fisiología animal
La señal BOLD está modulada por el latido cardiaco, la concentración de CO2 arterial y la temperatura. Existe una gran variedad de anestésicos que modulan diferentes dianas en el cerebro y que actúan sobre los receptores periféricos causando una regulación cardiaca y respiratoria. Por tanto, producirán distintos efectos sobre la señal BOLD y sobre otros parámetros hemodinámicos.
Por ejemplo: en una rata anestesiada con ventilación: donde paCO2, paO2 y pH se mantienen constantes, se víó una reducción del contraste T2* entre las venas y el parénquima cuando la rata estaba anestesiada con Isofluorano al 2% en lugar de medetomidina o ketamina/xylacina. Con el isofluorano se incrementa el CBF y la vasodilatación.
El mantener al animal ventilado hace que se evite la hipercapnia (aumento de paCO2) que tiene un efecto sobre la reproducibilidad del estudio fMRI . La hipercapnia también produce una vasodilatación y un incremento en el CBF. La variación del CBF puede explicar también una disminución especifica de la respuesta BOLD en la actividad neuronal inducida por un estímulo.
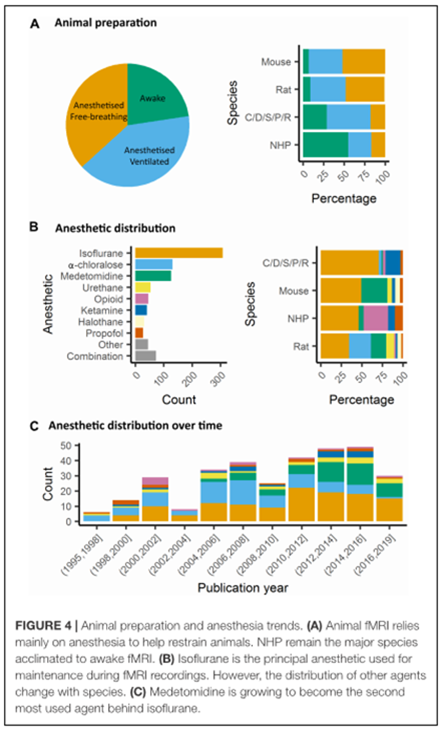
En la revisión, se han estudiado los efectos de diferentes anestésicos sobre la oxigenación sanguínea en diferentes regiones cerebrales. El impacto de la anestesia sobre otros parámetros fisiológicos, tales como la temperatura corporal y actividad cardiovascular periférica pueden modular la calidad de la conectividad funcional. El mantenimiento de estos parámetros pueden ser controlados y monitorizados. Otro de los parámetros que deben de ser controlados es la presión sanguínea.
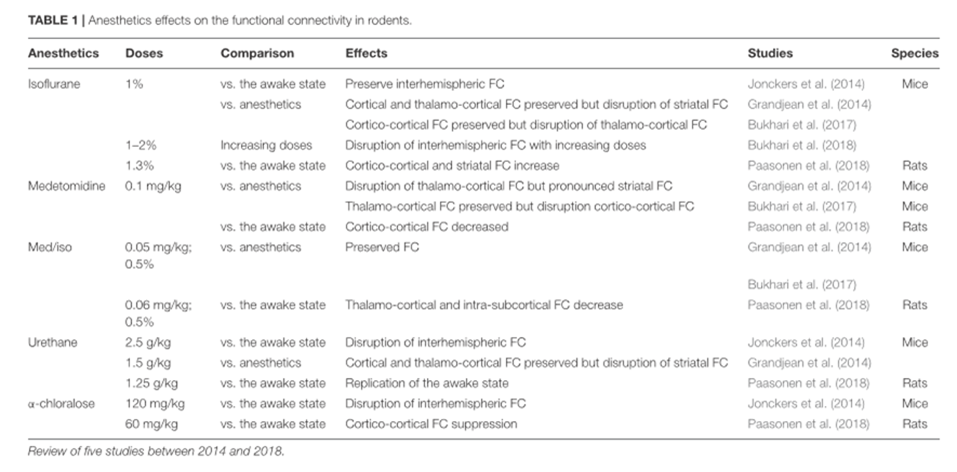
Los anestésicos empleados para los estudios con animales se han clasificado en función de su diana: los que actúan sobre los receptores GABAa, NMDA, canales de K+ .
Los más empleados son los que actúan a través de los receptores GABAa: son canales de Cl- que hiperpolarizan las neuronas, haciendo que sean menos excitables e inhibiendo los potenciales de acción. Los anestésicos más empleados son el Isofluorano, Propofol y barbitúricos. Cada fármaco actúa de distinta manera
El isofluorano y Sevofluorano tienen actividad metobólica opuesta en el flujo sanguíneo cerebral y distinto metabolismo de la glucosa en varias regiones del cerebro La alfa-cloralosa también es utilizada porque produce una buena respuesta metabólica y hemodinámica.
Otro de los antagonistas de los receptores de NMDA empleados es la ketamina que bloquea la actividad sináptica excitatoria. Produce un aumento de la actividad cerebral regional y un aumento del volumen sanguíneo cerebral. En roedores los más utilizados son el Isofluorano y la medetomidina
Adquisición de los datos
La actividad neuronal induce una vasodilatación en los capilares y arteriolas vecinas que se puede propagar hacia las arterias y venas. El aumento del CBF y CBV y la oxigenación de la sangre es en lo que se basa el principio de la fMRI. El método más común es el contraste BOLD: en el que se estudian las propiedades paramagnéticas de la deoxihemoglobina que produce un cambio en la susceptibilidad magnética dentro de los vasos sanguíneos y tejido vecino que es detectado por secuencias de T2 y T2*.
La [deoxiHb] aumenta desde las arterias (<5%) hacia las venas (40%) en el árbol vascular debido a la extracción del oxígeno de los capilares haciendo que la imagen BOLD sea particularmente sensible en los capilares, vénulas y venas. En el tejido cerebral sano, la actividad neuronal induce un aumento del CBF que produce un aumento de la entrega del oxigeno que excede sobre la disminución del oxigeno en los capilares. Como resultado, la [desoxiHb ] en los capilares y venas decrece, dando una señal BOLD positiva detectada en las imágenes de T2 y T2*.
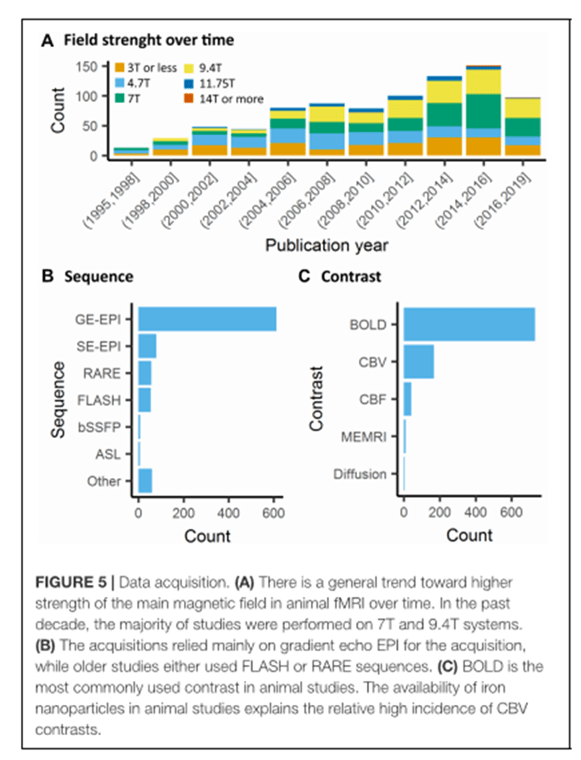
Las secuencias más empleadas en los estudios de fMRI en roedores son las de eco de gradiente pero es muy sensible a los artefactos de susceptibilidad, más en las cavidades cercanas a los oídos y bulbo olfatorio, particularmente cuando se utilizan tiempos de eco largos en campos magnéticos altos. Esta secuencia también es muy sensible a las venas grandes que hace que la secuencia no sea espacialmente precisa en los acoplamientos neurovaculares a nivel de los capilares. Para obtener una actividad neuronal espacial específica se usa la secuencia de eco de espin que es sensible a los vasos sanguíneos pequeños.
Aunque el contraste BOLD es el más empleado para hacer fMRI, otro de los métodos que sirve para calcular el CBV y/o el CBF es el empleo de agentes de contraste exógeno con partículas de óxido de hierro. Estas nanopartículas tienen una relajatividad r2 y r2* muy alta, no atraviesan la barrera hematoencefálica cuando está intacta y tienen un tiempo de circulación en sangre de horas. La administración intravenosa de éstas produce fenómenos de susceptiblidad magnética dentro de la vasculatura y en los tejidos de alrededor, que a una dosis alta tienen muchos más efectos que la deoxihemoglobina. Como resultado, la señal T2* intravascular apenas se detecta, mientras que la señal T2* extravascular se hace más sensible a los cambios en el CBV. Un incremento en el CBV, inducido por una actividad neuronal, aumenta la susceptibilidad magnética dentro del voxel, dando un contraste T2* negativo-CBV no dependiente. El contraste CBV es independiente del campo magnético y produce una bajada de la intensidad de la señal con respecto a la línea base cuando se inyecta una nanopartícula de óxido de hierro.
Aunque la mayoría de las técnicas de fMRI en animales están basados en la respuesta hemodinámica a la actividad neuronal, existen otros métodos más específicos para estudiar esta respuesta neuronal: como la imagen de difusión-fMRI y la que emplea Manganeso, pero estas técnicas lo dificultan por la limitada o no uniforme sensibilidad, baja resolución espacial y por dudas en los mecanismos subyacentes.
ANALISIS DE DATOS
Pre-procesamiento
Incluye una serie de pasos para corregir los artefactos y normalizar los datos: Corrección de movimiento, Filtro temporal, Co-registro a un patrón de referencia. Son muchos las herramientas que se utilizan para este primer paso, pero hasta la fecha no existe un método universal para todos los estudios que se realizan en diferentes centros, por lo que los métodos empleados hacen difícil compararlos entre ellos.
Selección de patrón y del atlas
El registro de los resultados de Fmri a una referencia común es uno de los pasos necesarios en el preprocesamiento y permite que el análisis sea imparcial a nivel de voxel.
En los estudios de animales se ha comprobado que este paso en la mayoría de ellos no se hace, a pesar de que este paso proporciona un registro óptimo para el contraste de la imagen, resolución y orientación, esto añade desafíos extra para compararlos entre estudios.
Analisis resting state
Para los estudios de Fmri con: estimulos provocados, farmacológicos, DBS y optognética/quimicogenetica, la mayoría de ellos son analizados con estadística a nivel de voxel donde las series de tiempo en cada voxel son tratados como modelos independientes, normalmente se ajusta a un modelo de respuesta hemodinámica frente a un paradigma de estimulo/inyección. A menudo se complemente con un análisis de ROIs.
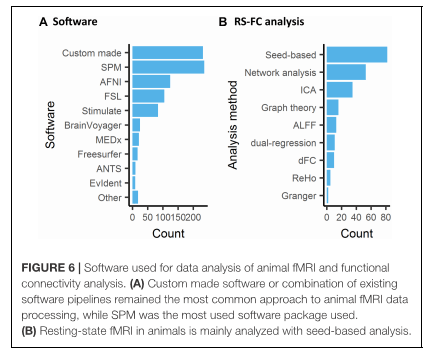
Como en en resting-state no se emplea un paradigma, se tienen que emplear modelos intrínsecos para estudiar la conectividad o medidas asociadas. Hay varios métodos de análisis que han sido desarrollados; primero en humanos pero que se pueden aplicar a los estudios con animales. Los análisis se basarían en hipótesis (crecimiento en semilla) hasta trabajar con los datos (análisis de componentes principales) y podrían ser aplicados a nivel de la red neuronal hasta un ROI en particular. Algunos métodos describen la relación entre áreas, otros se basan en las características de las variaciones a baja frecuencia de la señal BOLD en una sola región.
Bibliografía:
Animal Functional Magnetic Resonance Imaging: Trends and Path Toward Standardization Neuroinform., 22 January 2020: REVIEW ARTICLE
Un comentario en “Imagen de Resonancia magnética funcional fMRI”